北大團隊研發環狀RNA新冠疫苗 可中和Omicron等毒株較mRNA更優
面對新冠病毒不斷變異,能預防多種變種病毒的廣譜疫苗提供了更優的接種策略。據北京大學生命科學院消息,北大研究團隊研發的環狀RNA(Circular RNA,簡稱circRNA)新冠疫苗,可有效中和包括Omicron在內的多種變異株,且比mRNA疫苗更具優勢。
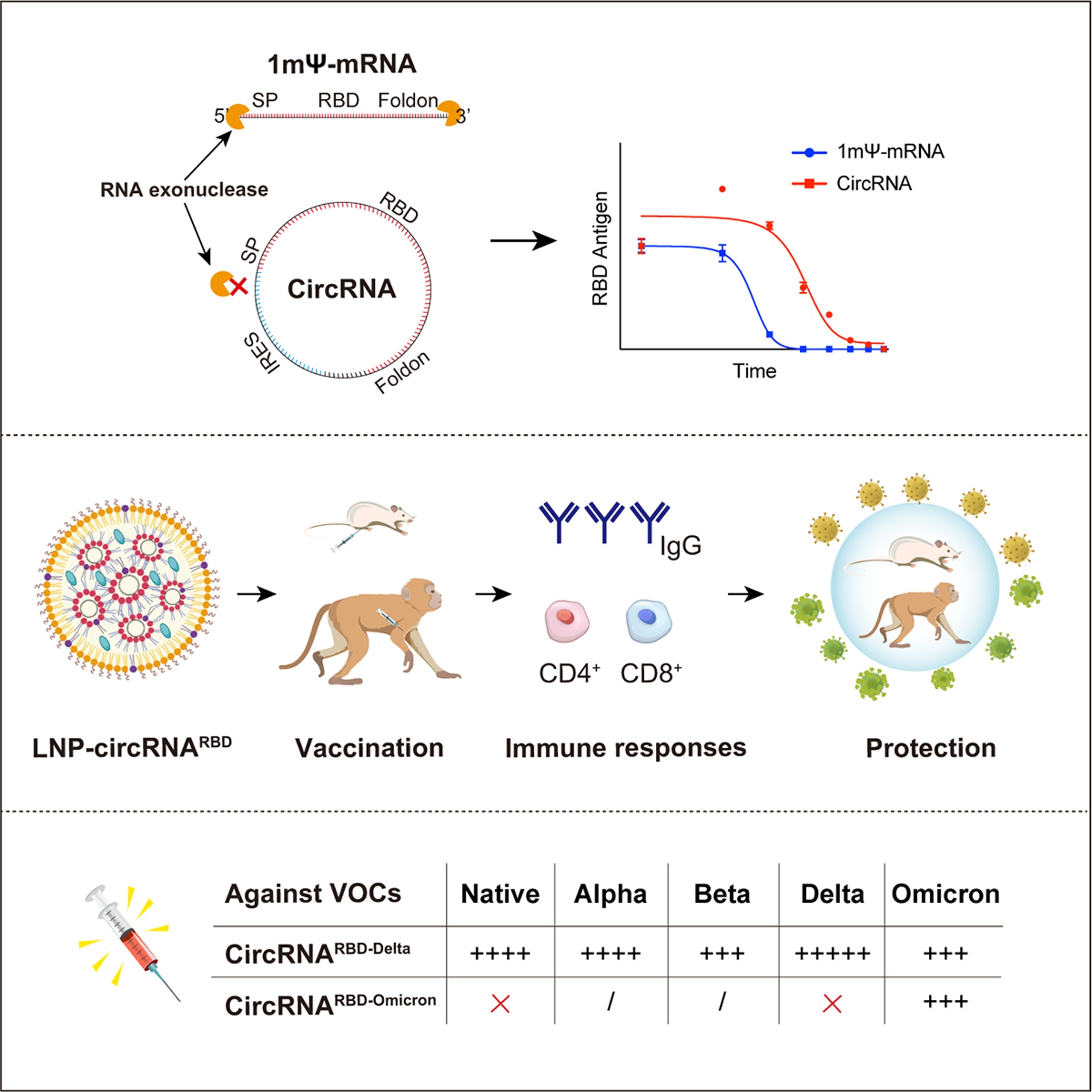
3月31日,北京大學魏文勝課題組在國際權威學術期刊《Cell》在線發表題為「Circular RNA Vaccines against SARS-CoV-2 and Emerging Variants」(針對SARS-CoV-2和新出現變異株的環狀RNA疫苗)的研究論文,首次報導了環狀RNA疫苗技術平台,以及據此開發的針對新冠病毒及其一系列變異株的環狀RNA疫苗。該項研究中製備的針對新冠病毒Delta變異株對多種新冠病毒變異株具有廣譜保護力。
研究團隊認為,傳統的滅活、病毒樣顆粒等疫苗平台已被用於開發新冠疫苗,且證明了安全性和有效性。作為近幾年興起的突破性醫學技術,mRNA疫苗的基本原理是通過脂納米顆粒(LNP)將mRNA導入體內來表達抗原蛋白,以刺激機體產生特異性免疫反應。新冠肺炎爆發後,莫德納的mRNA-1273、輝瑞/BioNTech的BNT162b2,這樣的針對性的mRNA疫苗在多種疫苗類型中脫穎而出。
研究團隊指,mRNA疫苗雖然具有生產速度快、成本低,並且能快速應對病毒變異等優點,但也存在一些短板,例如其儲存和運輸條件較為苛刻(零下70℃),並具有潛在的免疫原性副作用。相比之下,環狀RNA由於其共價封閉的環結構而高度穩定,這可以保護其免受外切酶介導的降解。此外,環狀RNA比線性mRNA更穩定,在哺乳動物細胞中,環狀RNA的中位半衰期至少比線性mRNA長2.5倍。
研究團隊通過對比評估發現,與mRNA疫苗相比,環狀RNA疫苗具有更高的穩定性,可以在體內產生更高水平、更加持久的抗原;誘導機體產生的中和抗體比例更高,可以更有效地對抗病毒變異,降低疫苗潛在的抗體依賴增強症(ADE)副作用;誘導產生的IgG2/IgG1的比例更高,表明其主要誘導產生Th1型保護性T細胞免疫反應,可以有效降低潛在的疫苗相關性呼吸道疾病(VAERD)副作用。
研究團隊研究發現,基於Omicron變異株的環狀RNA疫苗的保護範圍狹窄,其誘導產生的抗體只能夠中和Omicron變異株。而針對Delta變異株設計的環狀RNA疫苗則可以在小鼠體內誘導產生廣譜的中和抗體,有效中和包括Omicron在內的多種新冠變異株。




